Lección 2
Biomoléculas inorgánicas
Son todas las sustancias que carecen de átomos de carbono en su composición química, excepto el dióxido de carbono y el monóxido de carbono (CO2 y el CO).
Entre estas están:
- El Agua
- Los minerales
- Los gases
El agua
Es la sustancia química más abundante en la materia viva. El agua se encuentra en la materia viva en tres formas:
- Agua circulante (sangre, savia)
- Agua intersticial (entre las células, tejido conjuntivo)
- Agua intracelular (citosol e interior de los orgánulos celulares)
La cantidad de agua presente en los seres vivos depende de tres factores:
- Especie: los organismos acuáticos contienen un porcentaje muy elevado de agua mientras que las especies que viven en zonas desérticas tienen un porcentaje muy bajo.
- Edad del individuo: las estructuras biológicas de los organismos jóvenes presentan una proporción de agua mayor que las de los individuos de más edad.
- Tipo de tejido u órgano: dado que las reacciones biológicas se llevan a cabo en un medio acuoso, los tejidos con una gran actividad bioquímica contienen una proporción de agua mayor que los más pasivos.
Estructura química del agua
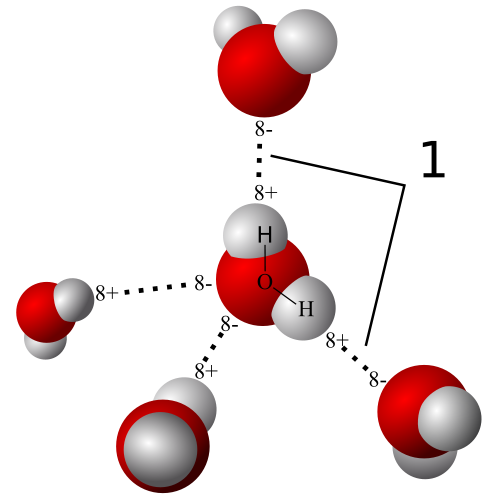
La molécula de agua está formada por la unión de un átomo de oxígeno y dos de hidrógeno mediante enlaces covalentes (cada átomo de H de una molécula comparte un par de electrones con el átomo de O).
La electronegatividad del O es mayor que la del H por lo que los electrones compartidos se desplazan hacia el átomo de O.
El O posee cuatro electrones más sin compartir, lo que tiene dos consecuencias:
- La geometría triangular de la molécula.
- La presencia de una carga negativa débil en la zona donde se sitúan los electrones no compartidos.
Sales minerales
Se pueden encontrar en los seres vivos haciendo parte de biomoléculas orgánicas, disueltas en agua o como minerales insolubles.
Sales inorgánicas insolubles en agua
Su función es de tipo plástico, formando estructuras de protección y sostén, como por ejemplo:
- Caparazones de crustáceos y moluscos (CaCO3) y caparazones silíceos de radiolarios y diatomeas
- Esqueleto interno en vertebrados (fosfato, cloruro, fluoruro y carbonato de calcio) y los dientes.
- Determinadas células incorporan sales minerales, como las que se pueden encontrar en la pared de celulosa de los vegetales, o como forma de producto residual del metabolismo (cristales de oxalato cálcico, que puede contribuir al desarrollo de cálculos renales o biliares)
- El carbonato de calcio también se puede encontrar en el oído interno, formando los otolitos que intervienen en el mantenimiento del equilibrio interno o partículas de magnetita que, al parecer, pueden utilizar algunos animales con función de brújula para orientarse en sus desplazamientos.
Sales inorgánicas solubles en agua
La actividad biológica que proporcionan se debe a sus iones y desempeñan, fundamentalmente, las siguientes funciones:

- Funciones catalíticas. Algunos iones como Mn+2, Cu+2, Mg+2, Zn+2, etc. actúan como cofactores enzimáticos siendo necesarios para el desarrollo de la actividad catalítica de ciertas enzimas . El ion ferroso-férrico forma parte del grupo hemo de la hemoglobina y mioglobina, proteínas encargadas del transporte de oxígeno.
- También el ion Mg+2 forma parte de las clorofilas y participa en los procesos de la fotosíntesis.
- El Ca+2, interviene en la contracción muscular y en los procesos relacionados con la coagulación de la sangre.
- Funciones osmóticas. Intervienen en la distribución del agua intra y extra celulares. Los iones Na+, K+, Cl-, Ca+2, participan en la generación de gradientes electroquímicos, que son imprescindibles en el potencial de membrana y del potencial de acción en los procesos de la sinapsis neuronal, transmisión del impulso nervioso y contracción muscular.
- Función tamponadora. Se lleva a cabo por los sistemas carbonato-bicarbonato y monofosfato-bifosfáto.
Gases
Los gases son sustancias que se mantienen en ese estado en temperatura y presión normales, es decir a 25°C y presión de 1 atm.
Los principales gases componentes de la vida son el Oxígeno y el Dióxido de Carbono.
Oxígeno
El oxígeno surgió como un subproducto de la vida a través de la actividad fotosintética, jugando un papel fundamental en la aparición del agua tras su combinación con hidrógeno. Así también para general el ozono en las capas altas de la atmósfera y actuar como filtro de la radiación solar de onda corta.
La importante labor del oxígeno en la tierra primitiva, permitió la colonización de los ecosistemas terrestres por parte de los primeros seres vivos que se habían formado en los océanos, los que de esta forma pudieron abandonar el agua. La presencia de oxígeno determinó también el desarrollo del proceso de respiración celular, mediante el cual se produce un intercambio de gases opuestos al de la fotosíntesis, contribuyendo a su equilibrio en la actual atmósfera. El desarrollo del ciclo del oxígeno en la Biosfera hizo posible la evolución de formas de vida multicelulares, incluido el hombre, al poder satisfacer sus necesidades energéticas a través de su metabolismo.

El oxígeno es entonces esencial para, ya que es el principal purificador, que se encarga de oxidar las toxinas y los desperdicios que genera el cuerpo para que el organismo pueda liberarse y deshacerse de ellos por medio de los órganos excretores, además, este elemento es necesario para transformar los carbohidratos, grasas y proteínas de la dieta en calor, energía, y vida. Este proceso es conocido como “metabolismo”. El oxígeno es el elemento esencial en los procesos respiratorios de la mayor parte de las células vivas.
Dióxido de carbono
Este gas imprescindible para la vida, forma parte de un intercambio permanente entre los seres vivos y la atmósfera. Los vegetales requieren un suministro continuo de dióxido de carbono, que a través de la fotosíntesis en las plantas verdes se combina para formar en último término glucosa y liberar oxígeno gaseoso. Este oxígeno es imprescindible para la vida tanto animal como vegetal, ya que en el proceso de respiración se vuelve a transformar en dióxido de carbono y agua. Respiración y fotosíntesis son dos procesos de óxido reducción complementarios.
Sin embargo, dado que este gas se genera muchas veces producto de una combustión, es muy frecuente que produzcamos mucha mayor cantidad de lo que es necesario. Esto ocasiona muchísimos problemas en el medio ambiente. El exceso de emisión de dióxido de carbono a la atmósfera es uno de los causantes del deterioro de la capa de ozono.


